
Vlad Krasen
1
941
113
Les scientifiques peuvent enfin comprendre la mystérieuse transition derrière une expérience de chimie centenaire. Les détails de cette transformation, dans laquelle l'ajout d'électrons à une solution d'ammoniac bleu vif la transforme en un bronze métallique brillant, ont longtemps échappé aux scientifiques..
La nouvelle étude révèle les détails subtils de ce changement et montre que cette transformation est graduelle plutôt que soudaine. «Ce que nous avons réussi, c'est que nous avons à peu près compris comment ces solutions se comportent à une large gamme de concentrations en utilisant une technique de micro-jet», a déclaré le co-auteur de l'étude Ryan McMullen, étudiant au doctorat en chimie à l'Université de Californie du Sud. . Cette technique, qui consiste à projeter des flux fins de la solution à travers un vide, n'a pas été utilisée sur le liquide brillant avant.
Et la découverte pourrait ouvrir de nouveaux types de réactions en chimie organique à l'avenir, a déclaré McMullen .
En relation: 8 éléments chimiques dont vous n'avez jamais entendu parler
Qu'est-ce qu'un métal?
Les métaux sont un groupe diversifié. Certains, comme le lithium, sont suffisamment légers pour flotter, tandis que d'autres, comme le plomb ou l'osmium, sont extrêmement denses. Certains nécessitent des températures incroyablement élevées pour fondre, tandis que d'autres fondent facilement (le mercure, par exemple, fond à moins 38,3 degrés Celsius ou moins 37,9 degrés Fahrenheit). En fin de compte, ce que les métaux ont en commun est leur capacité à conduire l'électricité au zéro absolu, le point auquel le mouvement moléculaire de la chaleur s'arrête essentiellement..
Mais comment certains non-métaux se transforment-ils en métaux? Dans une nouvelle étude, les chercheurs ont répondu à cette question en ajoutant des métaux à l'ammoniac liquide.
Premièrement, les chercheurs ont condensé l'ammoniac, qui est un gaz à température ambiante, en un liquide en le refroidissant à moins de 27,4 F (moins 33 C). Ils ont ensuite ajouté soit du sodium, du lithium ou du potassium, qui sont tous des métaux alcalins. (De manière assez célèbre, ces métaux réagissent de manière explosive lorsqu'ils sont immergés dans l'eau.) Les expériences ont été menées en collaboration avec des scientifiques de l'Académie tchèque des sciences et de l'Institut Fritz-Haber de la société Max Planck à Berlin, ainsi que des chercheurs japonais et français..
En relation: Le top 10 des plus grandes explosions de tous les temps
Le résultat était une réaction attendue: l'ammoniac liquide a tiré des électrons du métal. Ces électrons se sont ensuite retrouvés piégés entre les molécules d'ammoniac, créant les soi-disant électrons solvatés que les chercheurs espéraient étudier. À de faibles concentrations, le résultat était un liquide bleu non métallique. Au fur et à mesure que les électrons solvatés ou piégés s'accumulaient, la solution est passée au bronze brillant.
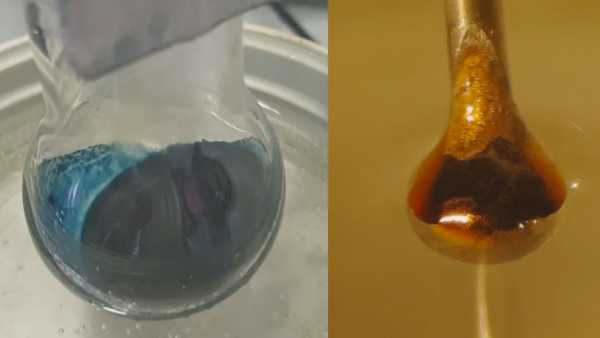
Le défi suivant était d'étudier comment les électrons solvatés se comportaient à différentes concentrations. Cela impliquait de projeter un microjet de la solution - environ la largeur d'un cheveu humain - à travers un faisceau de rayons X synchrotron, qui sont des faisceaux de rayons X à haute énergie. Les rayons X ont excité les électrons solvatés, les faisant sauter hors de leur cage liquide de molécules d'ammoniac. Les chercheurs pourraient alors mesurer la quantité d'énergie nécessaire pour libérer les électrons solvatés.
Les chercheurs ont découvert que plus la concentration d'électrons solvatés était élevée, plus le modèle de libération d'énergie correspondait à ce que l'on voit dans un métal. Voici ce que cela signifie: si vous tracez le graphique de la quantité d'énergie nécessaire pour libérer les électrons de leur cage d'ammoniac liquide, les métaux ont généralement ce qu'on appelle un «bord de Fermi», une transition très abrupte, a déclaré McMullen. À des concentrations plus faibles d'électrons solvatés, ce graphique de libération d'énergie ressemble plus à une colline arrondie. Ce n'est qu'à des concentrations d'électrons plus élevées que ce bord de Fermi est apparu. Le bord reflète la quantité d'énergie des électrons à une température donnée, a ajouté McMullen.
"Lorsque vous augmentez la concentration à la gamme métallique, alors vous voyez, ce motif merveilleux émerge qui est très, très caractéristique d'un métal", a déclaré McMullen.
Les résultats étaient intéressants car ils ont montré que le liquide de type métal créé en combinant les métaux alcalins et l'ammoniac est en fait un métal à un niveau physique fondamental, a-t-il déclaré..
"C'est un véritable métal, ce n'est pas quelque chose qui en ressemble à un", a déclaré McMullen.
Les électrons solvatés à plus faible concentration sont utilisés dans un type de réaction appelé réaction de Birch, qui ajoute des électrons à des structures moléculaires appelées anneaux aromatiques. Ce type de réaction a été utilisé dans la fabrication des premières pilules contraceptives orales dans les années 1950, a déclaré McMullen. En comprenant comment les électrons solvatés fonctionnent à des concentrations élevées, les chercheurs peuvent potentiellement trouver de nouveaux types de réactions chimiques, a-t-il déclaré. Par exemple, ils pourraient exciter les électrons solvatés avec des faisceaux de lumière pour les amener à se comporter de manière nouvelle.
"Si vous chatouillez un peu les électrons pour qu'ils soient plus énergiquement excités, vous pouvez commencer à regarder des réactions folles qui ne se produiraient jamais autrement", a déclaré McMullen.
Les chercheurs ont rapporté leurs résultats le 5 juin dans la revue Science.
Voir tous les commentaires (2)














